- Ce este un atom?
- Cum este alcătuit un atom?
- Cum se combină atomii?
- Părți ale unui atom
- Istoria atomului
- Moleculă
Vă explicăm ce este un atom și cum este alcătuită fiecare dintre părțile sale. De asemenea, istoria sa, studii despre ea și ce este o moleculă.

Ce este un atom?
Cea mai mică unitate care constituie materie.
Cuvântul atom provine din greaca veche (atom, „Fără diviziune”) și a fost inventat de primii filozofi pentru a teoretiza despre compoziția lucrurilor, adică particulele elementare ale univers. De atunci, odată cu apariția modele atomice, modul de a le imagina a variat enorm, pe măsură ce un model atomic i-a succedat celui precedent de-a lungul secolelor, până am ajuns la cel pe care îl folosim astăzi.
Atomii au proprietățile de element chimic care compun și, la rândul lor, elementele sunt organizate și clasificate în funcție de acestea numerele atomice, configurația electronică și proprietățile chimice în Tabelul periodic a elementelor.
Același element chimic poate fi compus din diferiți atomi din aceeași clasă, adică cu același număr atomic (număr de protoni pe care fiecare atom îl are în element), deși masele lor atomice sunt diferite.
De exemplu, există diferiți atomi ai aceluiași element care diferă prin numărul lor de neutroni, și se numesc izotopi, un caz reprezentativ sunt izotopii elementului carbon (12C, 13C, 14C). Deci, fiecare atom aparține aceluiași element chimic sau nu, în funcție de numărul său de protoni, deci atomii cu același număr de protoni aparțin aceluiași element chimic.
Cum este alcătuit un atom?
Atomii sunt formați dintr-un nucleu și unul sau mai mulți electroni (care au o sarcină negativă) în jurul acestuia. Nucleul este format din particule numite protoni și neutroni. Protonii sunt încărcați pozitiv, iar neutronii sunt neutri. Setul de protoni și neutroni se numește nucleoni.
Protonii și electronii sunt atrași unul de celălalt de forța electromagnetică (interacțiunea particulelor încărcate cu câmpurile electrice și magnetice), în timp ce protonii și neutronii sunt atrași unul de celălalt de forța nucleară (o forță experimentată doar de particulele care alcătuiesc nucleul atomic).
Cum se combină atomii?
Atomii se pot combina între ei pentru a forma legături chimice, ce se întâmplă când își împart electronii într-un fel sau altul. Legăturile chimice pot fi covalent, ionic Y metalic, care generează compuși moleculari covalenti, rețele ionice sau compuși metalici (deși este important de clarificat că nicio legătură chimică nu este absolut covalentă sau ionică). În acest fel, atomii se pot combina pentru a forma molecule simplu ca Apă, precum și a forma macromolecule complex ca proteină, ADN Y ARN.
Deși atomii se disting unii de alții datorită configurației particulelor lor, este, de asemenea, adevărat că toți atomii aceluiași element sunt exact identici: atomii de hidrogen din Soare Sunt la fel cu cei care alcătuiesc corpul nostru, iar atomii de carbon din corpul unui câine sunt identici cu cei care alcătuiesc un diamant. Diferența constă în modul în care atomii se combină pentru a constitui diferiții compuși chimici care alcătuiesc organele și sistemele de organe din creaturi vii, materialele generate în industrie, și toată materia care alcătuiește universul.
Părți ale unui atom
Atomii sunt formați din două părți esențiale:
- Nucleul. Aproximativ 99,94% din masa unui atom este concentrată în nucleu, unde se află protonii și neutronii (care împreună se numesc „nucleoni”), uniți prin forțe nucleare puternice, ceea ce împiedică protonii să se respingă între ei, având aceeași electricitate. încărca.
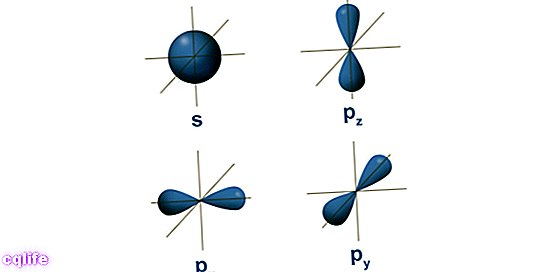
- Orbitalii atomici. Un orbital descrie o regiune a spațiului care înconjoară nucleul atomic în care probabilitate a găsi un electron este foarte mare. Aceste regiuni au forme diferite care se obțin ca rezultat al rezolvării ecuației staționare Schrödinger. Erwin Schrödinger a fost un om de știință austriac care a dezvoltat această ecuație în 1925 pentru a calcula evoluția unei particule subatomice, cum ar fi electronii. Astfel, electronii formează un fel de „nor” în jurul nucleului, care este reprezentat de forma orbitalilor atomici. Pe de altă parte, fiecărui orbital atomic îi corespunde o anumită valoare energetică pentru electroni, astfel încât aceștia sunt organizați în funcție de valorile lor energetice. Următoarea figură arată formele primilor orbitali atomici:
Istoria atomului

Primul care a formulat ideea existenței atomilor a fost filozoful grec Democrit (s.V-VI î.Hr.) din speculații pur imaginare (cum era înțeleasă știința la acea vreme).
Studiile sale au fost preluate de filozofi de mai târziu, precum Leucip și Epicur, dar au fost neglijate în timpul medieval, umbrită de explicația creaționistă a lumii, care atribuia totul lui Dumnezeu.
A trebuit să așteptăm până în 1773 când chimistul francez Antoine de Lavoisier și-a postulat teoria privind necrearea sau distrugerea materiei (ea doar transformă) sau Legea conservării masei, care i-a permis lui John Dalton să formuleze prima teorie atomică modernă în 1804.
Savanţii succesivi ai fizic si chimie s-au inspirat din munca sa de a propune sisteme mai bune și mai complexe pentru înțelegerea particulelor fundamentale ale materiei. Ulterior, au fost propuse noi modele atomice până la cele mai utilizate astăzi.
Structura contemporană acceptată este cea derivată din experimente de Rutherford în 1911, împreună cu formulările lui Niels Bohr, Schrödinger și Heisenberg.
Moleculă
O moleculă este cunoscută ca unirea a doi sau mai mulți atomi prin legături chimice pentru a forma o structură mai complexă și neutră din punct de vedere electric. Legăturile chimice pot fi covalente sau ionice.
Moleculele pot fi formate din atomi ai aceluiași element chimic, de exemplu, molecula de oxigen (O2), sau din atomi ai diferitelor elemente chimice, de exemplu, molecula de glucoză. Gazele monoatomice, de exemplu heliul (He), sunt de asemenea considerate molecule.

